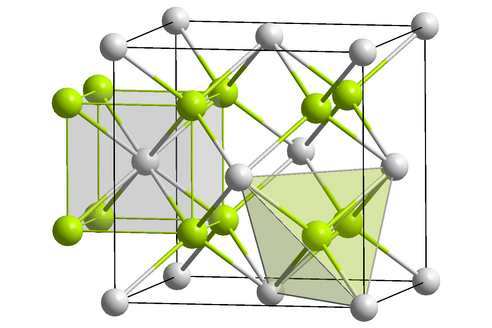
Fluorid samarnatý
Chemická sloučenina

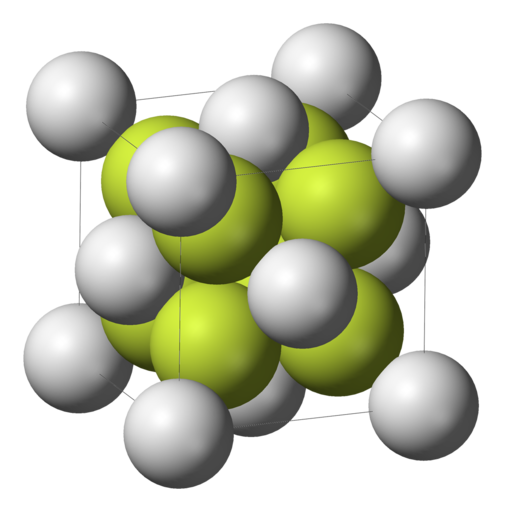
Fluorid samarnatý je anorganická sloučenina s chemickým vzorcem SmF2. Fluorid samarnatý je jedním z mála stabilních fluoridů vzácných zemin. Wikipedia
- Vzhledfialová až černá pevná látka
- Bod tání1417 °C
- Bod varu>2400 °C
- Molární hmotnost188,4 g/mol
Lidé také hledají
Fluorid samarnatý – Wikipedie
Fluorid samarnatý je anorganická sloučenina s chemickým vzorcem SmF2. Fluorid samarnatý je jedním z mála stabilních fluoridů vzácných zemin. [1 ]
Fluoridy – Wikipedie
Vzhledem k tomu, že fluor má největší elektronegativitu ze všech prvků, od kterých jsou známy nějaké sloučeniny (větší elektronegativitu mají jen helium a neon, od těch však nejsou známy žádné sloučeniny), jedná se převážně o iontové…
Fluorid sirnatý – Wikipedie
Fluorid sirnatý (SF2), též difluorid síry je anorganická sloučenina patřící mezi fluoridy. Snadno podléhá dimeraci insercí molekuly SF2 do vazby S-F za vzniku F3SSF. [1 ]
Fluorid strontnatý – Wikipedie
Fluorid strontnatý je téměř nerozpustný ve vodě. Dráždí oči a kůži a je škodlivý při vdechnutí nebo požití. Podobně jako fluorid vápenatý a fluorid barnatý vykazuje fluorid strontnatý při zvýšených teplotách superiontovou vodivost. [6…
Fluorid cínatý – Wikipedie
Fluorid cínatý je ve vodě snadno rozpustný, přičemž se hydrolyzuje. Při nižších koncentracích tvoří formy jako SnOH+, Sn(OH)2 a Sn(OH)3−. Při vyšších koncentracích vznikají převážně vícejaderné sloučeniny, například Sn2(OH)22+ and Sn3(OH)42…
Fluorid: padouch, nebo hrdina, po němž touží zubní sklovina…
Jsou fluoridy superhrdinové v boji proti kazu, nebo padouši stojící za skvrnami na zubech? Kdo by nechtěl znát pravdu! Čtěte dál a dozvíte se odpovědi na první poslední, co vás o fluoridech zajímá.
Neobsahuje samarnatýMusí obsahovat samarnatý
Fluorid sodný - Království-tianDe.cz
V současnosti preferovaná forma fluoridu, která má vysoce remineralizační účinky a zabraňuje tvorbě zubního kazu. Výhodou fluoridu sodného je jeho
Neobsahuje samarnatýMusí obsahovat samarnatý
Fluoridy – ano či ne? - Profimed.cz
Fluorid hraje velmi důležitou a nezastupitelnou roli v prevenci zubního kazu. Vzhledem ke své podstatě, sloučenina chemického prvku fluoru, má řadu příznivců i odpůrců. Jeho příměs se solí, vodou a kosmetickými přípravky je stále často…
Neobsahuje samarnatýMusí obsahovat samarnatý
Fluorit: Minerál s širokým využitím a jedinečnými vlastnostmi
Fluorit, známý také pod názvem kazivec, je minerál patřící do skupiny halogenidů s chemickým vzorcem CaF2 (fluorid vápenatý).
Neobsahuje samarnatýMusí obsahovat samarnatý
odkazuje na služby nejen od Seznam.cz.
© 1996–2025 Seznam.cz, a.s.